2021年12月30日,盛禾生物收到美国食品药品监督管理局FDA确认函,批准其全球创新生物药IAP0971进入临床,用于治疗晚期恶性实体瘤。IAP0971是盛禾生物基于自主知识产权专利强化抗体细胞因子(Armed ImmunoCytokine)AIC?平台研发的全球首个获批临床的同靶点抗体细胞因子。这也是继2021年12月10日FDA批准其IAE0972进入临床,盛禾生物又一基于AIC?平台研发的全球创新抗体细胞因子获批临床,展现了盛禾生物在免疫细胞因子领域的积累和创新。

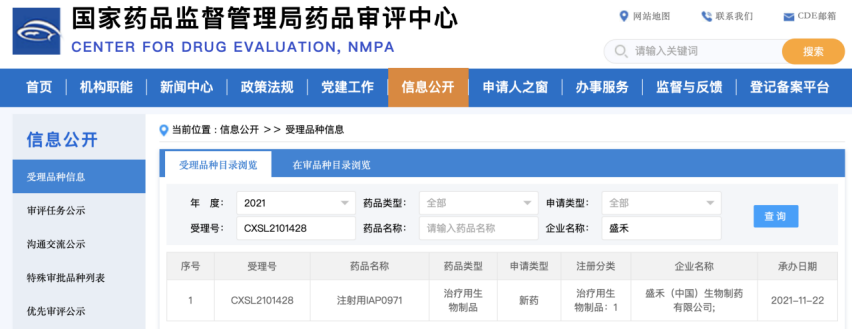
盛禾生物同步在中美递交IAP0971临床试验申请,并于11月30日获得FDA受理函,11月22日获得中国NMPA正式受理。
关于盛禾生物
盛禾(中国)生物制药有限公司(以下简称盛禾生物)位于南京经济技术开发区,是一家立足中国、面向全球的临床阶段的,以研发创新为驱动,聚焦肿瘤免疫领域、自身免疫性疾病和神经退行性疾病差异化创新抗体药物及抗体融合蛋白的研发、生产和商业化的创新型医药企业。盛禾生物布局具有自主知识产权的强化抗体细胞因子平台(AIC?)、强化天然免疫细胞多抗平台(AIM?),ADCC增强抗体平台(AEA?),以及其它创新药物形式。盛禾生物基于对免疫学、肿瘤微环境的深刻理解,充分调研未被满足临床需求,建立了20余全球创新和差异化研发管线,其中已有4个全球创新生物药进入临床研究阶段,4个进入临床申报阶段,6个进入临床前药学研究阶段,以及多个创新项目处于早期研发阶段。
盛禾生物拥有世界级抗体药物研发、工艺开发、质量研究、申报注册、生产和临床团队,其核心管理人员均有在国内外知名生物制药企业超过十年的产品研发和生产经验,带领团队完成多个靶向药物、创新生物药和生物类似药的研发和上市。盛禾生物拥有工艺开发、临床样品生产及商业化生产能力,具备完善的研发质量体系和GMP体系,符合美国食品药品监督管理局(FDA)、欧洲药品监管局(EMA)和中国食品药品监督管理总局(NMPA)的标准.盛禾生物拥有临床样品和商业化抗体药物原液生产车间和冻干粉针车间。抗体药物车间包括目前已经投入使用的1条1000L和3条200L的GMP原液生产线,以及正在安装调试中的5000L原液生产线。制剂生产车间具有1条水针灌装和1条冻干生产线,可以同时满足生物制品注射液和冻干粉针2种剂型的临床和商业化生产需要。盛禾生物着眼于全球药物市场,深耕免疫学和肿瘤微环境,重点布局全球创新抗体细胞因子,致力于解决未满足的临床需求,持续创新、追求卓越 ,努力成为国际一流的医药创新企业,研制革命性治疗药物,为人类健康努力奋斗。